AA-1800S石墨炉原子吸收测食品中的铅含量
发布时间:2024-07-10点击:次
本标准规定了食品中铅含量测定的石墨炉原子吸收光谱法、电感耦合等离子体质谱法、火焰原子吸收光谱法和二硫腙比色法。
本标准适用于各类食品中铅含量的测定。
试样消解处理后,经石墨炉原子化,在 283.3nm 处测定吸光度。在一定浓度范围内铅的吸光度值与铅含量成正比,与标准系列比较定量。
除非另有说明,本方法所用试剂均为优级纯,水为 GB / T6682 规定的二级水。
3. 1 试剂
3. 1. 1 硝酸( HNO 3 )。
3. 1. 2 高氯酸( HClO 4 )。
3. 1. 3 磷酸二氢铵( NH 4 H 2 PO 4 )。
3. 1. 4 硝酸钯[ Pd ( NO 3 ) 2 ]。
3. 2 试剂配制
3. 2. 1 硝酸溶液( 5+95 ):量取 50mL 硝酸,缓慢加入到 950mL 水中,混匀。
3. 2. 2 硝酸溶液( 1+9 ):量取 50mL 硝酸,缓慢加入到 450mL 水中,混匀。
3. 2. 3 磷酸二氢铵 - 硝酸钯溶液:称取 0. 02g 硝酸钯,加少量硝酸溶液( 1+9 )溶解后,再加入 2g磷酸二氢铵,溶解后用硝酸溶液(5+95 )定容至 100mL ,混匀。
3. 3 标准品
3. 4 标准溶液配制
3. 4. 1 铅标准储备液( 1000mg / L ):准确称取 1. 5985g (精确至 0. 0001g )硝酸铅,用少量硝酸溶液(1+9 )溶解,移入 1000mL 容量瓶,加水至刻度,混匀。
3. 4. 2 铅标准中间液( 1. 00mg / L ):准确吸取铅标准储备液( 1000mg / L ) 1. 00mL 于 1000mL 容量瓶中,加硝酸溶液(5+95 )至刻度,混匀。
3. 4. 3 铅标准系列溶液:分别吸取铅标准中间液( 1. 00mg / L ) 0mL 、 0. 500mL 、 1. 00mL 、 2. 00mL 、 3. 00mL和 4.00mL 于 100mL 容量瓶中,加硝酸溶液( 5+95 )至刻度,混匀。此铅标准系列溶液的质量浓度分别为 0 μ g / L 、5. 00 μ g / L 、 10. 0 μ g / L 、 20. 0 μ g / L 、 30. 0 μ g / L 和 40. 0 μ g / L 。
注:可根据仪器的灵敏度及样品中铅的实际含量确定标准系列溶液中铅的质量浓度。
注:所有玻璃器皿及聚四氟乙烯消解內罐均需硝酸溶液(1+5 )浸泡过夜,用自来水反复冲洗,最后用水冲洗干净。
4. 1 AA-1800S型原子吸收光谱仪(上海美析仪器有限公司):配石墨炉原子化器,附铅空心阴极灯。
4. 2 分析天平:感量 0. 1mg 和 1mg 。
4. 3 可调式电热炉。
4. 4 可调式电热板。
4. 5 微波消解系统:配聚四氟乙烯消解内罐。
4. 6 恒温干燥箱。
4. 7 压力消解罐:配聚四氟乙烯消解内罐。
5. 1 试样制备
注:在采样和试样制备过程中,应避免试样污染。
5. 1. 1 粮食、豆类样品样品去除杂物后,粉碎,储于塑料瓶中。
5. 1. 2 蔬菜、水果、鱼类、肉类等样品样品用水洗净,晾干,取可食部分,制成匀浆,储于塑料瓶中。
5. 2 试样前处理
5. 2. 1 湿法消解
称取固体试样 0.2g~3g (精确至 0.001g )或准确移取液体试样 0.500mL~5. 00mL 于带刻度消化管中,加入 10mL 硝酸和 0.5mL 高氯酸,在可调式电热炉上消解(参考条件: 120 ℃ / 0. 5h~1h ;升至180℃ / 2h~4h 、升至 200℃~220℃ )。若消化液呈棕褐色,再加少量硝酸,消解至冒白烟,消化液呈无色透明或略带黄色,取出消化管,冷却后用水定容至 10mL ,混匀备用。同时做试剂空白实验。亦可采用锥形瓶,于可调式电热板上,按上述操作方法进行湿法消解。
5. 2. 2 微波消解
称取固体试样 0.2g~0. 8g (精确至 0. 001g )或准确移取液体试样 0. 500mL~3. 00mL 于微波消解罐中,加入 5mL 硝酸,按照微波消解的操作步骤消解试样,消解条件参考附录 A 。冷却后取出消解罐,在电热板上于 140℃~160℃ 赶酸至 1mL 左右。消解罐放冷后,将消化液转移至 10mL 容量瓶中,用少量水洗涤消解罐 2 次 ~3 次,合并洗涤液于容量瓶中并用水定容至刻度,混匀备用。同时做试剂空白试验。
5. 2. 3 压力罐消解
称取固体试样 0.2g~1g (精确至 0.001g )或准确移取液体试样 0.500mL~5. 00mL 于消解内罐中,加入 5mL 硝酸。盖好内盖,旋紧不锈钢外套,放入恒温干燥箱,于 140℃~160℃ 下保持 4h~5h 。冷却后缓慢旋松外罐,取出消解内罐,放在可调式电热板上于 140℃~160℃ 赶酸至 1mL 左右。冷却后将消化液转移至 10mL 容量瓶中,用少量水洗涤内罐和内盖 2 次 ~3 次,合并洗涤液于容量瓶中并用水定容至刻度,混匀备用。同时做试剂空白试验。
5. 3 测定
5. 3. 1 仪器参考条件(AA-1800S)
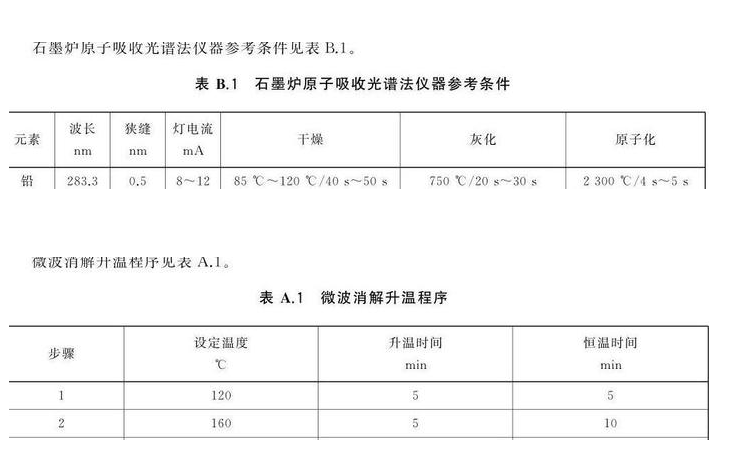
5. 3. 2 标准曲线的制作
按质量浓度由低到高的顺序分别将 10 μ L 铅标准系列溶液和 5 μ L 磷酸二氢铵 - 硝酸钯溶液(可根据所使用的仪器确定最佳进样量)同时注入石墨炉,原子化后测其吸光度值,以质量浓度为横坐标,吸光度值为纵坐标,制作标准曲线。
5. 3. 3 试样溶液的测定
在与测定标准溶液相同的实验条件下,将 10 μ L 空白溶液或试样溶液与 5 μ L 磷酸二氢铵 - 硝酸钯溶液(可根据所使用的仪器确定最佳进样量)同时注入石墨炉,原子化后测其吸光度值,与标准系列比较定量。
试样中铅的含量按式(1 )计算:
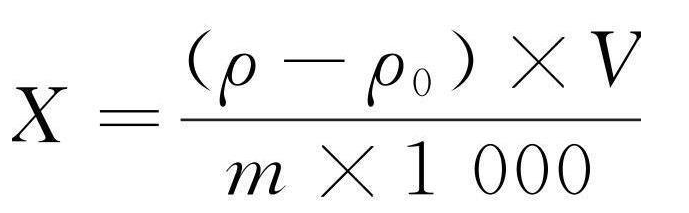
…………………………( 1 )
式中:
X———试样中铅的含量,单位为毫克每千克或毫克每升(mg/kg或mg/ L );
ρ———试样溶液中铅的质量浓度,单位为微克每升(μ g/ L );
ρ 0———空白溶液中铅的质量浓度,单位为微克每升(μ g/ L );
V———试样消化液的定容体积,单位为毫升( mL );
m———试样称样量或移取体积,单位为克或毫升(g 或 mL );
1000 ———换算系数。
当铅含量 ≥1.00mg/kg (或 mg/ L )时,计算结果保留三位有效数字;当铅含量
见 GB5009.268 。
试样经处理后,铅离子在一定pH条件下与二乙基二硫代氨基甲酸钠( DDTC )形成络合物,经 4- 甲基 -2- 戊酮( MIBK )萃取分离,导入原子吸收光谱仪中,经火焰原子化,在 283.3nm 处测定的吸光度。在一定浓度范围内铅的吸光度值与铅含量成正比,与标准系列比较定量。
注:除非另有说明,本方法所用试剂均为分析纯,水为 GB / T6682 规定的二级水。
10. 1 试剂
10. 1. 1 硝酸( HNO 3 ):优级纯。
10. 1. 2 高氯酸( HClO 4 ):优级纯。
10. 1. 3 硫酸铵[( NH 4 ) 2 SO 4 ]。
10. 1. 4 柠檬酸铵[ C 6 H 5 O 7 ( NH 4 ) 3 ]。
10. 1. 5 溴百里酚蓝( C 27 H 28 O 5 SBr 2 )。
10. 1. 7 氨水( NH 3 · H 2 O ):优级纯。
10. 1. 8 4- 甲基 -2- 戊酮( MIBK , C 6 H 12 O )。
10. 1. 9 盐酸( HCl ):优级纯。
10. 2 试剂配制
10. 2. 1 硝酸溶液( 5+95 ):量取 50mL 硝酸,加入到 950mL 水中,混匀。
10. 2. 2 硝酸溶液( 1+9 ):量取 50mL 硝酸,加入到 450mL 水中,混匀。
10. 2. 3 硫酸铵溶液( 300g / L ):称取 30g 硫酸铵,用水溶解并稀释至 100mL ,混匀。
10. 2. 4 柠檬酸铵溶液( 250g / L ):称取 25g 柠檬酸铵,用水溶解并稀释至 100mL ,混匀。
10. 2. 5 溴百里酚蓝水溶液( 1g / L ):称取 0. 1g 溴百里酚蓝,用水溶解并稀释至 100mL ,混匀。
10. 2. 6 DDTC 溶液( 50g / L ):称取 5gDDTC ,用水溶解并稀释至 100mL ,混匀。
10. 2. 7 氨水溶液( 1+1 ):吸取 100mL 氨水,加入 100mL 水,混匀。
10. 2. 8 盐酸溶液( 1+11 ):吸取 10mL 盐酸,加入 110mL 水,混匀。
10. 4 标准溶液配制
10. 4. 1 铅标准储备液( 1000mg / L ):准确称取 1. 5985g (精确至 0. 0001g )硝酸铅,用少量硝酸溶液(1+9 )溶解,移入 1000mL 容量瓶,加水至刻度,混匀。
10. 4. 2 铅标准使用液( 10. 0mg / L ):准确吸取铅标准储备液( 1000mg / L ) 1. 00mL 于 100mL 容量瓶中,加硝酸溶液(5+95 )至刻度,混匀。
注:所有玻璃器皿均需硝酸(1+5 )浸泡过夜,用自来水反复冲洗,最后用水冲洗干净。
11. 1 AA-1800C型原子吸收光谱仪(上海美析仪器有限公司):配火焰原子化器,附铅空心阴极灯。
11. 2 分析天平:感量 0. 1mg 和 1mg 。
11. 3 可调式电热炉。
11. 4 可调式电热板。
12. 1 试样制备同 5.1 。
12. 2 试样前处理同 5.2. 1
12. 3 测定
12. 3. 1 仪器参考条件(AA-1800C)
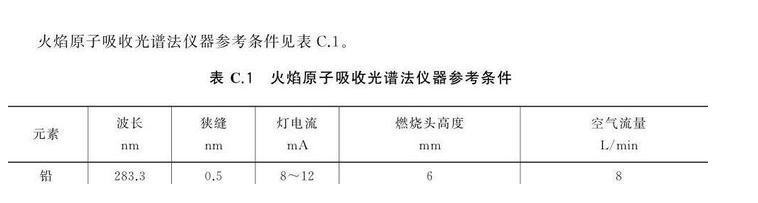
12. 3. 2 标准曲线的制作
分别吸取铅标准使用液 0mL 、 0.250mL 、 0. 500mL 、 1. 00mL 、 1. 50mL 和 2. 00mL (相当 0 μ g 、2. 50 μ g 、 5. 00 μ g 、 10. 0 μ g 、 15. 0 μ g 和 20. 0 μ g 铅)于 125mL 分液漏斗中,补加水至 60mL 。加 2mL 柠檬酸铵溶液(250g/ L ),溴百里酚蓝水溶液(1g/ L )3 滴 ~5 滴,用氨水溶液( 1+1 )调pH至溶液由黄变蓝,加硫酸铵溶液(300g/ L )10mL , DDTC 溶液( 1g / L ) 10mL ,摇匀。放置 5min 左右,加入 10mLMIBK ,剧烈振摇提取 1min ,静置分层后,弃去水层,将 MIBK 层放入 10mL 带塞刻度管中,得到标准系列溶液。将标准系列溶液按质量由低到高的顺序分别导入火焰原子化器,原子化后测其吸光度值,以铅的质量为横坐标,吸光度值为纵坐标,制作标准曲线。
12. 3. 3 试样溶液的测定
将试样消化液及试剂空白溶液分别置于 125mL 分液漏斗中,补加水至 60mL 。加 2mL 柠檬酸铵溶液(250g/ L ),溴百里酚蓝水溶液(1g/ L )3 滴 ~5 滴,用氨水溶液( 1+1 )调pH至溶液由黄变蓝,加硫酸铵溶液(300g/ L )10mL , DDTC 溶液( 1g / L ) 10mL ,摇匀。放置 5min 左右,加入 10mL MIBK ,剧烈振摇提取 1min ,静置分层后,弃去水层,将 MIBK 层放入 10mL 带塞刻度管中,得到试样溶液和空白溶液。将试样溶液和空白溶液分别导入火焰原子化器,原子化后测其吸光度值,与标准系列比较定量。
13 分析结果的表述
试样中铅的含量按式(2 )计算:
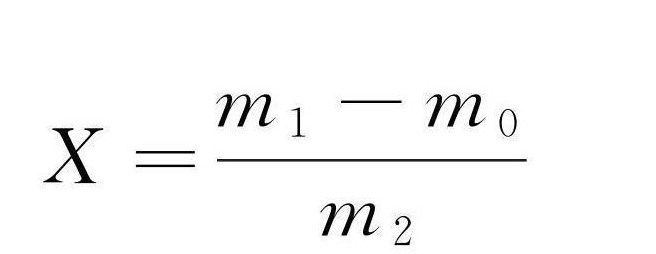
…………………………( 2 )
式中:
X ———试样中铅的含量,单位为毫克每千克或毫克每升(mg/kg或mg/ L );
m 1 ———试样溶液中铅的质量,单位为微克(μ g );
m 0 ———空白溶液中铅的质量,单位为微克(μ g );
m 2 ———试样称样量或移取体积,单位为克或毫升( g 或 mL )。
当铅含量 ≥10.0mg/kg (或 mg/ L )时,计算结果保留三位有效数字。

